本文
「知の拠点あいち」重点研究プロジェクトにおいて、がんの個別化医療を実現する検査装置を開発しました!~それぞれの患者さんに最適な肺がん治療を実現します~
愛知県は、公益財団法人科学技術交流財団に委託して大学などの研究シーズを企業の製品化・事業化につなげる産学行政連携の共同研究開発プロジェクト『「知の拠点あいち」重点研究プロジェクト』※1を実施しています。
このたび、プロジェクトの1つである「超早期診断技術開発プロジェクト」※2において、名古屋大学大学院工学研究科馬場嘉信教授、同医学系研究科長谷川好規教授らの研究グループは、独自の微細構造を持つ診断チップ「イムノウォールチップ」を開発し、がんの原因となるタンパク質を低コスト(従来法比100分の1)・迅速(同1,000倍)・高感度(同10倍)で調べることに成功しました。
がんの原因は、ダメージを受けた遺伝子からできた異常なタンパク質です。したがって、患者さんに最適な治療を提供するためには、どのタンパク質の異常ががんの原因になっているかを調べることが重要です。現在は、遺伝子をコピーして増やし、ダメージの場所を調べる方法が行われていますが、高コストで長時間を要することが問題となっています。
本開発品は、遺伝子ではなくタンパク質を調べます。ダメージを受けた遺伝子からできたタンパク質は、正常な遺伝子からできたものと比べると、分子構造が微妙に異なります。この違いを認識し、異常なタンパク質だけを検出することで、がんの原因を特定します。
イムノウォールチップは、異常タンパク質を捕捉する10億個もの抗体を特許出願中の独自技術によりマイクロ流路内に超高密度に固定したプラスチックチップで、低コスト・迅速・高感度な異常タンパク質の捕捉・検出を実現しました。
現在、名古屋大学大学院医学系研究科・呼吸器内科で、肺がん患者さんに対して行われているEGFR遺伝子検査※3(分子標的薬※4の効果を投薬前に調べる検査)の代替検査法としての利用を検討して、臨床試験を進めています。また、同脳神経外科においても、脳腫瘍手術への応用を検討しています。どちらの臨床医からも非常に高い評価を得ています。
今後、肺がんや脳腫瘍、大腸がん、乳がんなどの超早期診断への応用も実施の予定です。
1 開発の背景
がんの検査はこれまで、検体を検査会社に送り数万円、数週間を使って遺伝子を分析することが一般的でした。しかし、迅速・低コストな検査法が確立されれば、これまでの技術では不可能だった、スピードが問題となる手術中の診断や、コストが問題となる多項目同時診断などが可能になります。また、患者さんの身体的・経済的負担を軽減し、ひいては日本の医療費問題にも貢献できます。さらに、高コストが原因で先進国と同じ手法の検査を行えない新興国への普及も期待されます。
こうしたニーズに対応するため、名古屋大学大学院工学研究科馬場教授、笠間研究員が、ベッドサイドで素早く・高感度・低コストで調べられる検査チップを実用化し、臨床医である名古屋大学大学院医学系研究科長谷川教授らとともに、肺がん患者さんの検体を使って実証試験を進めてきました。その結果、本開発品が抗がん剤の治療効果を検証する上で、極めて有効であることが実証されました
2 本開発装置の概要
(1)従来の検査技術
がんの検査は、検査会社で広く用いられている遺伝子を調べるPCR※5ベースの手法と、近年開発されたタンパク質を調べるELISA※6(エライザ)法があります。
【PCRベースの手法】
一般的に検体の中のがん細胞由来のDNAは正常細胞由来のDNAと比較して圧倒的に少ないため、まずPCR法によって選択的にがん細胞由来のDNAを増幅しなければ分析できません。しかし、PCR法に使われる試薬は高価で、また増幅には数時間必要です。
【ELISA法】
プラスチック製の大きなウェル(くぼみ)の中で、抗原抗体反応※7によって目的のタンパク質を検出します。しかし、ウェルが比較的大きいため、多量(100~200 mL)の検体や試薬を必要とします。臨床現場では、極僅かな量(~10 mL)の検体しか採取できない場合も多々あり、このような検体を分析するのは極めて困難です。また、多量の試薬は低コスト化の妨げとなります。さらに、結果が出るまでに長時間を要する(一般に数時間~1日)ため、ベッドサイド診断やその場診断への応用は困難です。
(2)本開発装置の構成
本開発装置は、抗原抗体反応によって異常なタンパク質を捕捉する「イムノウォール」を有するマイクロ流路チップ(図1)と、捕捉されたタンパク質を蛍光によって検出する「蛍光検出器」(図2)からなり、蛍光検出器は高度な光検出技術を有する浜松ホトニクス(株)(本社 浜松市)によって試作されました。


マイクロ流路チップは、量産可能で安価なプラスチックで、1枚あたりのサイズが
25 mm×90 mm×5 mm、マイクロ流路(幅1 mm×長さ10 mm×深さ40 mm)を有し、その中にわずか高さ40 mm、幅40 mmのイムノウォールが形成されています。この構造は、名古屋大学大学院工学研究科が有する微細加工技術によって開発されました。
イムノウォールには、異常なタンパク質だけを捕捉する抗体が超高密度に固定化(特願2015-060845、PCT/JP2016/58447)されており、マイクロ流路という超微小な空間で抗原抗体反応を行います。分子の無駄な拡散を抑えることができるため、迅速な分析が可能となっています。また、試料や試薬も微量で済むため、わずかな検体(~1 mL)を低コストで分析することができます。
蛍光を検出することで検査結果を調べられます。蛍光検出器は、図2に示すようにコンパクトで軽量(約1 kg)、安価で、ベッドサイドにも設置可能ですが、実験室で用いられる蛍光顕微鏡と同程度の蛍光検出感度を持っています。
(3)本開発装置の測定手順
測定は、「イムノウォールチップ」により異常なタンパク質を選択的に捕捉する分析ステップと、異常なタンパク質が捕捉されたことを蛍光検出器によって確認する診断ステップに分かれています。
分析ステップでは、「イムノウォールチップ」に検体、試薬、洗浄液を順に入れます。これらの液の出し入れには、市販のマイクロピペットと吸引器を使います。その他特別な道具は必要ありません。測定方法の流れを図3に示します。流路に検体、抗体、蛍光標識抗体を順に入れます。それぞれの液に浸しておく時間は、数分(5~15分)、30秒、30秒です。液の入れ替えの間と分析ステップの最後には、流路内の洗浄を行います。洗浄には1回あたり約1分30秒かかります。この結果、一度の測定は最長でも20分程度です。
診断ステップでは、分析ステップが終わった「イムノウォールチップ」の蛍光検出を行います。蛍光検出器の観察ステージにイムノウォールチップを乗せて、装置の中に押し込みます。あとは、ソフトウェア上で「測定」ボタンを押すだけで、約1分でイムノウォールチップの蛍光を測り、検体の中に遺伝子変異タンパク質が存在するかどうかを自動で判定します。

3 肺がんに対する抗がん剤の有効性検証
(1)肺がんの現状
がん患者さんの数は世界中で急速に増加し、早期診断や新規治療法の開発等によるがん死亡の減少が人類にとっての大きな課題となっています。我が国においても平成26年には、367,943人が悪性新生物で死亡しており、男女とも死因の第一位となっています。悪性新生物の中では肺がんが第一死因であり、現在も急増するなど、その対策が重要です(図4)。
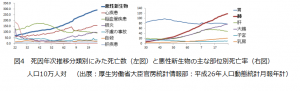
肺がんは小細胞肺がん※8と非小細胞肺がん※9に大別されます。非小細胞肺がん患者さんのうち、遺伝子変異型EGFRという異常なタンパク質が原因となっている患者さんの割合は、日本人を含むアジア人に特に高くなっています(肺がん10人中3~4人程度)。近年、このタイプの肺がんに対して、極めて効果が高い抗がん剤(分子標的薬)が市場に投入され、数々の治療実績が示されています。ただし、この分子標的薬を投与する際には、事前にがん細胞の遺伝子検査を行い、EGFR遺伝子型を詳細に調べるように肺がん診療ガイドラインで推奨されています。この遺伝子検査は、高価な検査費用(1検体あたり数万円~)と1週間程度の検査時間が必要で、患者さんの経済的負担となるばかりでなく、迅速な治療の妨げとなっています。
(2)肺がんに対する抗がん剤の有効性検証の結果(名大医生命倫理委員会承認番号2014-0171)
名古屋大学大学院医学系研究科呼吸器内科から提供された肺がん患者さん15人の胸水※10を本開発装置により分析を行った結果、15人で従来の検査法による診断結果と一致しました(一致率100%)。
(3)開発した検査法の優位性
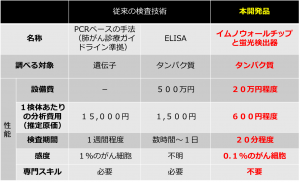
4 今後の展開
肺がんを対象とした研究において、分析する検体数を数百まで拡大し、本開発品の有効性を確認し、数年後の実用化を目指します。さらに、脳腫瘍を始めとする他のがんについても、実証試験を新たに開始する予定です。最終的には、国の認証を得て、病院等への導入を進める予定です。また、本開発品を新興国へと輸出し、遺伝子検査を身近なものとして広めていくことも検討しています。さらに、肺がんや脳腫瘍、大腸がん、乳がんなどの超早期診断への応用も実施していきます。
5 問合せ先
・プロジェクト全体に関すること
あいち産業科学技術総合センター 企画連携部
(1)担 当:鹿野、村上
(2)所 在 地:豊田市八草町秋合1267番1
(3)電 話:0561-76-8306
(4)F A X:0561-76-8309
公益財団法人科学技術交流財団 知の拠点重点研究プロジェクト統括部
(1)担 当:冨田、安部、村山、山本
(2)所 在 地:豊田市八草町秋合1267番1
(3)電 話:0561-76-8380
(4)F A X:0561-21-1653
・本開発装置に関すること
名古屋大学
(1)担 当:大学院工学研究科 教授 馬場嘉信、研究員 笠間敏博
(2)所 在 地:名古屋市千種区不老町1
(3)電 話:052-789-3560
(4)F A X:052-789-4666
用語説明
※1 「知の拠点あいち」重点研究プロジェクト
高付加価値のモノづくりを支援する研究開発拠点「知の拠点あいち」を中核に実施している産学行政の共同研究開発プロジェクト。大学などの研究シーズを企業の製品化へつなげる橋渡しの役割を担う。
※2 超早期診断技術開発プロジェクト
(プロジェクトリーダー)名古屋大学学術研究・産学官連携推進本部 特任教授 太田美智男
(内容)超高齢化社会において、全国的に増加が予想される脳・循環器系疾患、がん、生活習慣病を早期に発見するために、工学系の研究者と医学系の研究者(医師)が医工連携体制を構築し、痛みがない、少ない、簡易な早期診断技術や日常的な健康モニタリング技術を確立する。
(参加機関)18大学6公的研究機関16企業(うち中小企業8社)
大学:名古屋大学、名古屋工業大学、豊橋技術科学大学、愛知県立大学、愛知学院大学、愛知工業大学、椙山女学園大学、中部大学、中京大学、豊田工業大学、名古屋市立大学、藤田保健衛生大学、京都工芸繊維大学、大阪市立大学、三重大学、広島大学、広島市立大学、北海道大学
公的研究機関:(国研)国立長寿医療研究センター、(国研)産業技術総合研究所、愛知県がんセンター、(公財)愛知県健康づくり振興事業団、あいち産業科学技術総合センター、(公財)科学技術交流財団
企業:(株)医学生物学研究所、(株)スズケン、高砂電気工業(株)、(株)槌屋、(株)デンソー、(株)NAST、ブラザー工業(株)、(株)ユネクス、(株)LIXIL、(株)オプトニクス精密、中央精機(株)、東レ(株)、日本ケミコン(株)、浜松ホトニクス(株)、フィガロ技研(株)、(株)ユニテック
※3 EGFR遺伝子検査
細胞に存在するタンパク質「上皮成長因子受容体(EGFR)」の情報をコードしている遺伝子について、ダメージの位置を調べる検査。
※4 分子標的薬
近年注目されている抗がん剤の一種。がん細胞の特定の分子に結合するなどして増殖や成長を阻害し、自死を誘引する。
※5 PCR
ポリメラーゼ連鎖反応。目的の遺伝子だけを増幅する技術。
※6 ELISA
酵素が結合された抗体によって抗原を検出および定量する分析方法。
※7 抗原抗体反応
抗原とそれに対応する抗体との特異的な結合。
※8 小細胞肺がん
肺の入り口に近い太い気管支に多く発生する肺がん。肺がん全体の20%程度。
※9 非小細胞肺がん
肺の深部に多く発生する肺がん。化学療法と放射線療法があまり有効でない。肺がん全体の80%程度で、本邦で最も発生数が多い。
※10 胸水
胸膜腔内に貯留する異常量の体液。肺や胸膜の炎症や感染、がんなどの疾患のほか、心不全や肝硬変などが原因となる。

